ArbutusBiopharma:在研乙肝新药AB-729停药12周后仍观察到HBsAg强劲下降
AB-729是ArbutusBiopharma公司采用专有GalNAc技术递送技术开发的一款可皮下注射(SC)使用的RNA干扰(RNAi)疗法药物,临床前模型中AB-729减少所有HBV转录本,从而实现抑制病毒复制和减少乙肝表面抗原(HBsAg),目前该药正在健康受试者和慢乙肝患者中进行Phase1a/1b期临床试验。
在本届美国肝病学会年(AASLD2020)上,研究人员报告了该药物在正在进行的首次人体临床试验在慢乙肝患者中使用AB-729后的初步安全性和药效学(PD)结果。

该项Phase1a/1b期临床试验的第一部分研究了单剂量AB-729或安慰剂在健康受试者中的作用。
在第二部分中,目前正在接受核苷(酸)类似物进行抗病毒治疗、非肝硬化、HBeAg阳性或阴性、HBVDNA低于检测下限、ALT高达5xULN的慢性乙型肝炎患者接受单剂量60mg、90mg或180mg的AB-729用药治疗,评估包括用药后至少12周的安全性和药效学(PD)结果。
第三部分是对不同剂量水平/间隔的AB-729多剂量方案进行为期6个月的评估。
研究结果显示,到目前为止,还没有严重的不良事件(AEs)或由于AEs而中断的情况出现。
在第二部分,在16名服用药物的慢性乙型肝炎患者中观察到19次不良反应,其中大部分是轻度的。11/19被评估为具有相关性的;其中7例是与注射有关的轻度到中度的不良反应(主要是疼痛)。
剂量为180mg时,在出现急性胃肠炎的情况下,有2名受试者出现短暂的1级ALT升高和1名受试者出现无相关性的3级ALT/AST升高。60mg和90mg队列中所有受试者的ALT/AST水平保持正常或与研究前水平相同(在1名受试者中)。
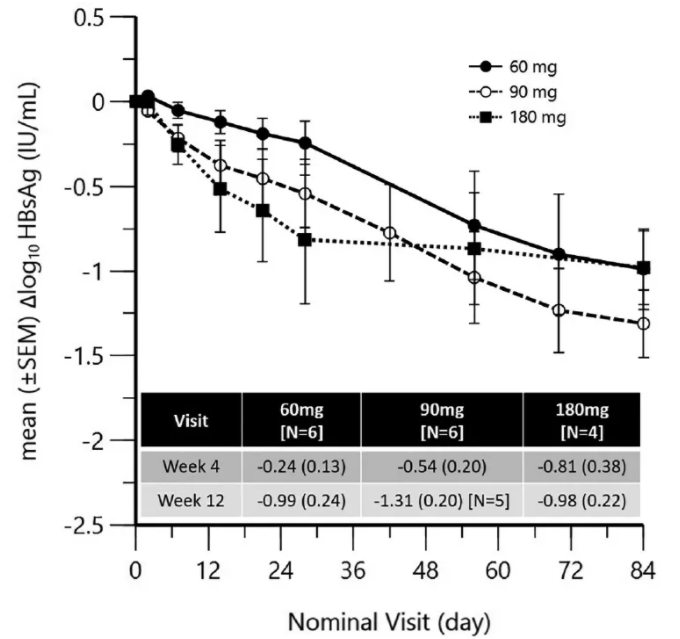
在单剂量AB-729用药后,在用药12周后观察到平均乙肝表面抗原(HBsAg)继续下降(如图)。在第12周时,HBsAg的下降范围为-0.62至-2.14log10(60mg),-0.79至-1.87log10(90mg)和-0.69至-1.62log10(180mg)。
正在进行每4周和每8周一次给药间隔的60mgAB-729评估,并将报告可用的安全性和PD数据。
综上数据,研究认为,在单次SC剂量后,AB-729通常是安全且耐受性良好的,在60mg和90mg人群中,ALT/AST没有临床相关变化。在慢乙肝受试者中,单剂量60mg,90mg和180mg用药后12周,仍持续观察到平均HBsAg强劲下降,这些数据支持在多剂量研究中每月一次或更短的给药间隔。(更多肝病新药研究信息敬请关注“肝脏时间”微信公众号)!
信息源:
SAFETYANDPHARMACODYNAMICSOFTHEGALNACsiRNAAB-729INSUBJECTSWITHCHRONICHEPATITISBINFECTION
声明: 不要轻信任何医疗广告或新闻报道式广告! 请勿轻信素未谋面的网络医生! 本站所刊载的信息仅供参考,不能代表医生的诊断和治疗,请勿直接对照治疗而延误病情! 因个人主职工作时间不宽裕,网站未来仅保持不定期更新。










全部评论:暂无评论