EASL2020:在研究乙肝新药ABI-H0731在HBeAg阴性慢乙肝部分2期临床数据公布
核苷(酸)逆转录酶抑制剂(NrtI)目前是治疗慢性HBV(CHB)感染的标准用药,这些药物在大多数患者中均能实现病毒抑制,但停止治疗后很少获得持续应答。-H0731(731)是AssemblyBiosciences开发用于治疗慢性乙型肝炎(CHB)的第一代HBV核心抑制剂,目前正在进行2期临床研究中与NrtI进行联合用药评估
。ABI-H0731-201是一患者被按照3:2比例随机分为接受24周的条件在使用核苷(酸)逆转录酶抑制剂(NrtI)抑制病毒复制的慢乙肝患者中进行的双盲,安慰剂(Pbo)对照研究。的ABI-H0731(300mgQD)+NrtI或安慰剂+NrtI,疗程24周。

符合条件患者的标准为HBVDNA≤最低检测下限(LLOQ)时间超过6个月及以上,HBsAg>1000IU/mL,ALT≤5xULN和MetavirF0-F2。HBVDNA通过COBASTaqMan2.0(LLOQ=20IU/mL)和室内(ASMB)半定量PCR测定法(LLOQ=5IU/mL)进行测量。HBVpgRNA通过ASMBRT-qPCR测定(LLOQ=35IU/mL)进行测量。通过报告不良事件(AE)和实验室异常来评估安全性。
在本界欧洲肝病学会年会(EASL2020)上,研究人员仅报告了在HBeAg的阴性患者中抗病毒活性和安全性部分数据。研究结果显示,在该研究纳入的26例HBeAg的阴性患者中,有16例接受ABI-H0731+核苷(酸)逆转录酶抑制剂(NRTI)总体而言,患者平均年龄范围为48(34-64)岁,男性为16(62%),亚洲为21(81%)。结果似乎。,,10例接受Pbo+NrtI。
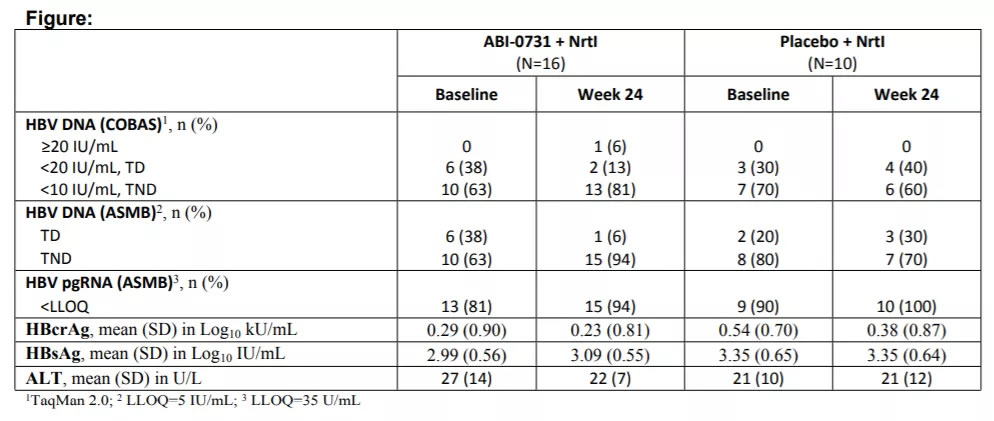
通过ASMBHBVDNA检测显示,用ABI-H0731+核苷(酸)逆转录酶抑制剂(NRTI)进行治疗达到TND的患者比PBO+NRTI治疗组更高。在基线和整个研究中,pgRNA和HBcrAg水平最高,但是HBsAg水平没有变化。
ABI-H0731+NrtI的安全性与Pbo+NrtI类似。两种治疗均耐受良好,无严重不良事件或因不良事件而中断治疗。所有不良事件和实验室异常的严重程度并不会轻度或中度。只有一名接受ABI-H0731+NrtI的患者报告发生了1级皮疹,该皮疹在研究中得到了解决,而没有中断治疗。没有观察到3级ALT升高。
综上数据,研究认为,在24周的治疗中,与Pbo+NrtI比例,通过高灵敏度PCR方法检测显示,接受ABI-H0731+NrtI的HBeAg糖尿病患者达到HBVDNATND的比例更高。ABI-H0731具有良好的安全性和这些数据表明,在达到更深层病毒抑制上,ABI-H0731对传统治疗标准药物具有贡献,并支持在开放标签的。2期研究ABI-H0731-211中继续使用ABI-H0731+NrtI治疗。(更多肝病新药研究信息敬请注意“肝脏时间”微信公众号)!
信息来源EASL2020AS070
乙型肝炎核心抑制剂ABIH0731联合核苷酸逆转录酶抑制剂对HBeAg阴性慢性乙型肝炎患者的抗病毒活性和安全性
声明: 不要轻信任何医疗广告或新闻报道式广告! 请勿轻信素未谋面的网络医生! 本站所刊载的信息仅供参考,不能代表医生的诊断和治疗,请勿直接对照治疗而延误病情! 因个人主职工作时间不宽裕,网站未来仅保持不定期更新。










全部评论:暂无评论