EASL2020:在研乙肝新药GS-9688部分2期临床随访研究结果公布
Selgantolimod(GS-9688,SLGN)是一种由GileadSciences公司开发的慢乙肝治疗的选择性口服小分子TLR8兴奋剂,目前正在缓慢乙肝患者中进行2期期临床试验,在本界欧洲肝病学会年会(EASL2020)上,新西兰研究人员报告了该药用药第48周后(Selgantolimod用药24周后)的安全性和有效性研究结果。

将患者随机分为2组(HBeAg阳性和阴性),分别接受每周3mg,1.5mg和安慰剂(PBO)(2:2:1)治疗,共24周,期间持续使用口服抗病毒药物用药。安全评估包括监测不良事件(AE)和实验室异常。主要疗效终点是第24周时HBsAg水平的平均下降幅度≥1log10IU/mL的患者比例。次要终点包括HBsAg和HBeAg阴转的患者比例以及药效(PD)标志物包括细胞因子(IL)如IL-1RA和IL-12p40和免疫细胞亚群评估(使用光谱流式细胞仪进行评估(覆盖髓样,T,B和NK细胞亚群)。
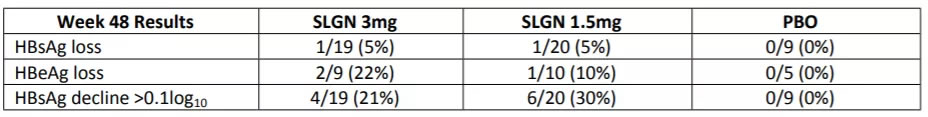
随机分配48例患者(24例HBeAg阳性和24例阴性))各组的基线特征相似:。大多数是亚洲人(58%),男性(75%),平均(SD)年龄为47(9)岁,平均的HBsAg为2.9(1.1)LOG10IU/mL的表中显示了第48周时的血清学应答。
在第48周,Selgantolimod组中HBsAg阴转,HBeAg阴转和HBsAg下降相对于安慰剂组更为明显,Selgantolimod组中21-30%的患者HBsAg下降≥0.1log10IU/mL。
在该研究中,没有患者出现病毒学突破。3mgSelgantolimod组或安慰剂组中没有3级或4级不良反应。1.5mg组中有3例患者发生3级AE,均未导致早期停药。报告频率最高的(Selgantolimod治疗组的定义为≥20%)不良事件(Selgantolimodv安慰剂)为:恶心(46%v0),上呼吸道感染(URTI)(23%v33%),头痛(21%v44%),呕吐(23%v0)和疲劳(21%v11%)。胃肠道疾病多为轻度和短暂性。
研究观察到细胞因子随药物剂量呈比例增加。
Selgantolimod用药后第4小时,第1天和第23天的中值(IQR)IL-12p40,3mg组,1.5mg组和安慰剂组分别为6.0(3.9-10.4)和6.9(4.7-8.2),3.0(1.9-4.4)和3.9(2.9)-4.9),0.9(0.8-1.0)和1.0(0.9、1.0)pg/mL。在Selgantolimod治疗的24周内未观察到快速耐受(速激肽)。
具有血清学应答的患者的进一步免疫学表征转化中。
综上数据,研究据认为每周一次口服高达3mg的Selgantolimod,持续24周,是安全且耐受性良好的。剂量补充药效学变化和未观察到快速耐受,支持Selgantolimod每周一次用药。在第24周的随访中,观察到2例患者HBsAg阴转,3例患者HBeAg阴转。(更多肝病新药研究信息敬请关注“肝脏时间”微信公众号)!
AS071
在病毒抑制下的成人慢性乙型肝炎患者中,口服TLR8激动剂selgantolimod进行24周治疗的有效性和安全性:一项2期研究
声明: 不要轻信任何医疗广告或新闻报道式广告! 请勿轻信素未谋面的网络医生! 本站所刊载的信息仅供参考,不能代表医生的诊断和治疗,请勿直接对照治疗而延误病情! 因个人主职工作时间不宽裕,网站未来仅保持不定期更新。











全部评论:暂无评论