为何有支持免疫耐受期慢乙肝患者进行抗病毒治疗的声音?
编者按:以往有研究认为基于拉米夫定(LAM)、普通干扰素α(IFNα)和恩曲他滨等药物治疗免疫耐受期(IT)慢乙肝患者,免疫应答情况不佳,不推荐对IT患者进行抗病毒治疗。然而逐渐有新的研究发现IT患者肝脏病理情况不佳。
随着医学理念的不断进步,治疗方案的不断优化,基于现有核苷和干扰素α类药物进行抗病毒治疗的IT患者应答良好且远期结局可获得显著改善,慢慢出现了支持IT患者进行抗病毒治疗的声音。对此问题的争议也成为了慢乙肝治疗的热点和难点。肝霖君今天将为大家分享支持IT患者进行抗病毒治疗的最全证据。

现阶段,各指南对于IT的定义存在差异(如图),且均推荐对年纪较轻的IT患者进行监测,只有在组织学上有明显的炎症或纤维化时才进行抗病毒治疗。2017年EASL指南对IT患者的适应症更宽泛,建议30岁以上或有肝癌/肝硬化家族史的IT患者接受治疗,而2018年AASLD指南建议40岁以上的患者,尤其是组织学证据表明有明显肝脏组织学进展的患者考虑开展治疗。所有指南均建议对不符合治疗指征的患者进行监测,以便患者在达到治疗指征时及时开始抗病毒治疗。
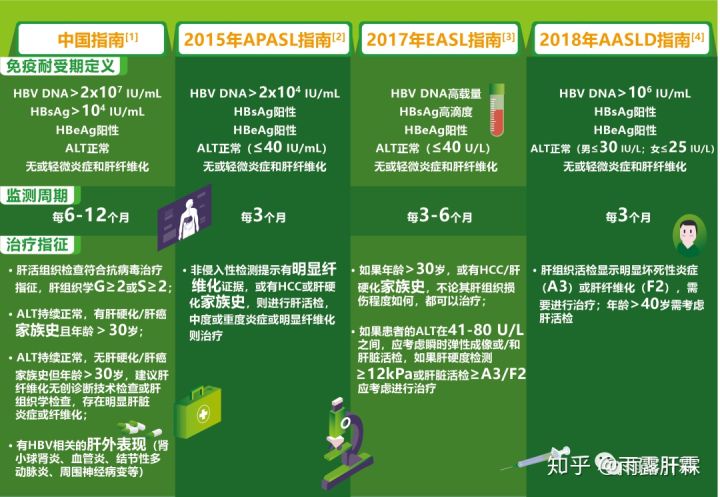
1. 免疫耐受期患者仍存在显著肝脏病理学变化
延安大学附属医院有证据[5]表明,IT患者仍存在显著肝脏病理学变化,研究纳入161例IT患者,其中肝脏炎症≥ G2者高达53.2%,纤维化≥ S2者占20.9%。
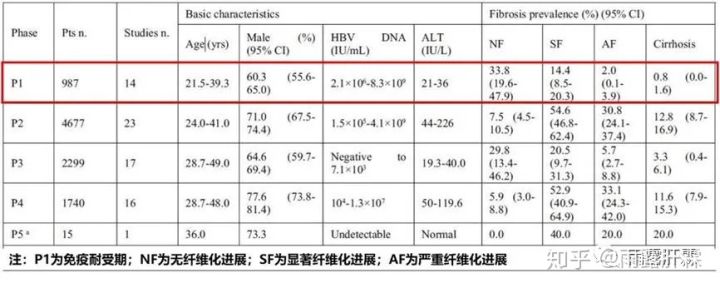
一项最新的荟萃分析纳入1988年-2018年文献库中乙肝自然史中肝纤维化进展的相关研究[6],分析发现其中987例IT患者中只有33.8%无肝纤维化进展,其余均有轻微或显著肝脏病理学变化。
以往肝霖君曾推出系统综述:
发现临床上部分慢性HBV感染者,尽管ALT正常,但在行肝穿刺活检时,肝组织均有显著肝脏炎症、纤维化,甚至达到早期肝硬化。基于全球范围内,慢乙肝抗病毒治疗覆盖率极低,其中限制性的治疗建议也进一步降低了治疗率。若单纯根据ALT升高水平和HBV DNA水平来判断是否进行抗病毒治疗,可能导致许多ALT正常患者错失治疗时机。
因此,从预防组织学进展的角度来讲,IT患者应积极进行抗病毒治疗。
2. 未治疗的免疫耐受期患者有肝癌和死亡高风险
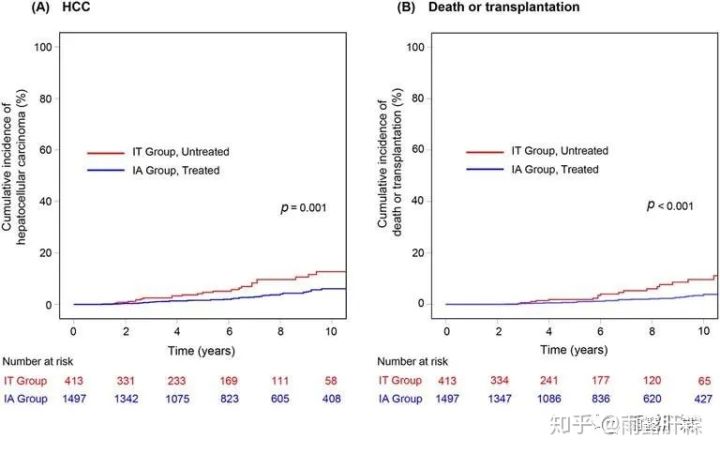
Gut上发表的一项韩国研究[7]比较未治疗的IT患者和治疗的免疫活动期(IA)患者的累积肝癌发生率和死亡/移植发生率,发现未治疗的IT患者显著更高。多因素分析显示:未治疗的IT患者比接受治疗的IA患者有更高的肝癌发生风险(10年:12.7% vs. 6.1%;P = 0.001)。未治疗的IT患者比接受治疗的IA患者有更高的死亡率或肝移植率(10年:9.7% vs. 3.4%;P< 0.001)
中国台湾对围产期感染HBV的患者进行的一项大规模研究[8]显示,在30岁时,肝癌的发生就已经急剧上升。围产期感染HBV的特点是延长了IT持续时间。事实上,慢乙肝患者发生肝癌的时间可能早于30岁,表明肝癌的癌变过程可能始于IT。
Gastroenterology上一项新加坡的研究证实了这一点[9],发现IT患者体内出现高水平的HBV DNA整合和克隆性肝细胞扩增,这表明即使在早期慢性HBV感染患者中,肝癌的发生也可能正在进行。
3. 免疫耐受期儿童患者抗病毒治疗后应答情况良好
解放军总医院第五医学中心的朱世殊教授等发表在Journal of Hepatology上的一项研究[10]纳入69例中国2-16岁儿童IT患者,随机2:1分为基于干扰素α治疗组(干扰素α单药或干扰素α序贯联合核苷治疗)和未治疗组。基于干扰素α治疗组HBV DNA转阴率、HBeAg血清学转换率和HBsAg清除率均显著高于未治疗组(73.91% vs. 0%; 32.6% vs. 4.35%; 21.74% vs. 0%)。所有患者无严重不良反应发生。
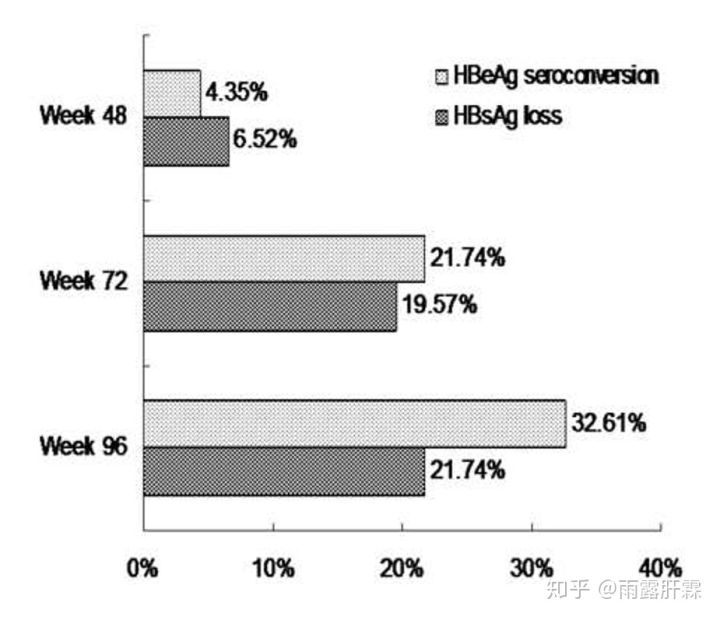
一项来自英国的研究[11]显示,核苷序贯/联合干扰素α治疗23例儿童IT患者,78%的患者获得HBV DNA清除,22%的患者获得了HBeAg血清学转换,17%的患者同时获得了病毒学抑制和HBsAg血清学转换。
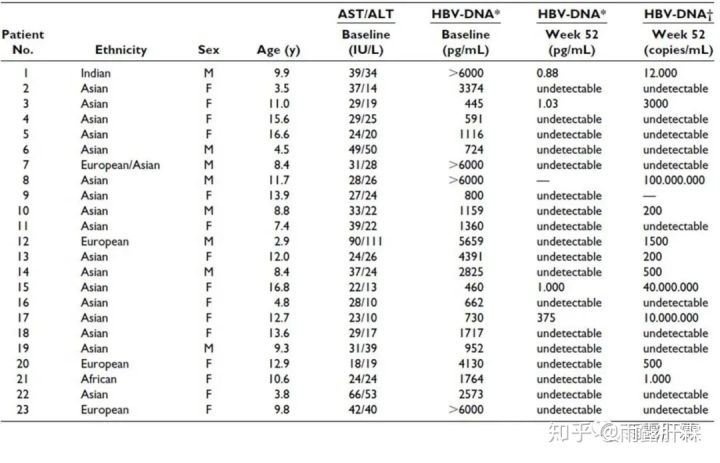
印度研究团队的一项研究[12]再次验证了这个结果,纳入28例儿童IT患者进行抗病毒治疗(核苷序贯/联合干扰素α)和34例儿童患者不治疗,两组进行肝穿的患者中F0期肝纤维化占比无显著性差异(68% vs. 64%, P = 0.73)。治疗组HBeAg血清学转换率显著高于未治疗组(39.3% vs. 5.9%, P = 0.006),HBsAg清除率也高于未治疗组(21.4% vs. 5.9%),治疗组所有患者均获得了病毒学抑制。
因此,对于儿童IT患者开始抗病毒治疗的研究证据相当充分,且多是基于干扰素α的研究。以往我们也有很多儿童慢乙肝患者采用基于聚乙二醇干扰素α治疗的获得更高的临床治愈率的相关报道
尽早治疗,尽早获得临床治愈,获得远期结局的改善。
4. 免疫耐受期患者抗病毒治疗具成本效益
一项比较从免疫耐受期开始抗病毒治疗与延迟到免疫活性期进行治疗的成本效益的研究[13]显示,从医疗保健系统的医疗成本上来看,IT患者开始抗病毒治疗处于高成本效益的边界;但从社会角度来看,加上生产力损失的成本,从IT期开始抗病毒治疗是一种占优势地位的策略。
肝霖君有话说
IT患者是否应该进行抗病毒治疗一直存在争议,而各国指南对于IT患者的定义也不尽相同,主要体现在HBV DNA不同水平的定义。AASLD2018和2019年中国指南对于IT患者HBV DNA的定义均较高,分别为大于106 IU/mL和 2 x 107 IU/mL,而APASL2015的定义却较低(> 2 x 104 IU/mL),EASL2017对HBV DNA水平没有明确界定,且大部分指南对于HBsAg滴度无明显界定,这就导致临床上对IT患者的界定不清,部分关于抗病毒治疗IT患者应答不佳的研究可能也是基于不同IT定义导致治疗方案的选择不恰当所致,所以基于此开展的关于IT患者的研究也得出一些矛盾的结论。
但是现有很多证据发现IT患者存在显著肝脏病理学变化,且有肝癌或死亡高风险,这部分人群在现有优化的抗病毒治疗方案治疗下,也可获得较高的免疫应答率。现有许多儿童IT患者基于干扰素α治疗获得较高应答率的证据,这是很受鼓舞的,与其守株待兔,承担免疫耐受期可能进展为免疫活动期等状态的风险,不如尽早治疗,尽早治愈,降低远期肝癌风险。当然对于IT患者的治疗证据也需要更多的研究来证实,特别是对于成人患者。在慢乙肝临床治愈已能较好实现的今天,对特殊患者的关注应该更多。
参考文献:
[1] Chinese Society of Infectious Diseases CMA, Chinese Society of Hepatology CMA. Guidelines for the prevention and treatment of chronic hepatitis B (version 2019)[J]. J Clin Hepatol, 2019, 35(12): 35(12).
[2] Sarin SK, Kumar M, Lau GK, et al. Asian-Pacific clinical practice guidelines on the management of hepatitis B: a 2015 update[J]. Hepatol Int, 2016, 10(1): 1-98.
[3] European Association for the Study of the Liver. Electronic address eee, European Association for the Study of the L. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection[J]. J Hepatol, 2017, 67(2): 370-398.
[4] Terrault NA, Lok ASF, McMahon BJ, et al. Update on prevention, diagnosis, and treatment of chronic hepatitis B: AASLD 2018 hepatitis B guidance[J]. Hepatology, 2018, 67(4): 1560-1599.
[5] 高红艳, 刘娜, 李春霞, et al. 慢性乙型肝炎病毒感染者免疫耐受期的临床特征与肝组织病理学分析[J]. 肝脏, 2018, 23(02): 136-139.
[6] Wang Y, Lin MH, Li HQ. Histologic fibrosis across the natural course of chronic hepatitis B virus infection: a systematic review and meta-analysis[J]. Liver Int, 2020, 2020 APAPS Abstract (1359).
[7] Kim GA, Lim YS, Han S, et al. High risk of hepatocellular carcinoma and death in patients with immune-tolerant-phase chronic hepatitis B[J]. Gut, 2018, 67(5): 945-952.
[8] Beasley RP, Hwang LY, Lin CC, et al. Hepatocellular carcinoma and hepatitis B virus. A prospective study of 22 707 men in Taiwan[J]. Lancet, 1981, 2(8256): 1129-1133.
[9] Mason WS, Gill US, Litwin S, et al. HBV DNA Integration and Clonal Hepatocyte Expansion in Chronic Hepatitis B Patients Considered Immune Tolerant[J]. Gastroenterology, 2016, 151(5): 986-998 e984.
[10] Zhu S, Zhang H, Dong Y, et al. Antiviral therapy in hepatitis B virus-infected children with immune-tolerant characteristics: A pilot open-label randomized study[J]. J Hepatol, 2018, 68(6): 1123-1128.
[11] D'Antiga L, Aw M, Atkins M, et al. Combined lamivudine/ interferon-alpha treatment in "immunotolerant" children perinatally infected with hepatitis B: a pilot study[J]. J Pediatr, 2006, 148(2): 228-233.
[12] Poddar U, Yachha SK, Agarwal J, et al. Cure for immune-tolerant hepatitis B in children: is it an achievable target with sequential combo therapy with lamivudine and interferon?[J]. J Viral Hepat, 2013, 20(5): 311-316.
[13] Kim HL, Kim GA, Park JA. Anti-viral treatment in patients with immune tolerant-phase chronic hepatitis B may be cost-effective[J]. Journal of Hepatology, 2019, EASL 2019 ( Abstract FRI182 ).
声明: 不要轻信任何医疗广告或新闻报道式广告! 请勿轻信素未谋面的网络医生! 本站所刊载的信息仅供参考,不能代表医生的诊断和治疗,请勿直接对照治疗而延误病情! 因个人主职工作时间不宽裕,网站未来仅保持不定期更新。











全部评论:暂无评论